La infección por el temido VIH, el virus que causa el sida, es cada vez más fácil de controlar en el mundo, pero imposible de curar; o casi imposible porque esta regla tiene dos excepciones.
La primera excepción es Timothy Ray Brown, de Estados Unidos, residente en Berlín (Alemania), portador del virus y quien si bien logró vivir por más de 10 años gracias al uso de medicamentos antirretrovirales, entró en peligro de muerte por una leucemia no relacionada con este intruso.
El asunto, según los artículos de la época, es que para tratar este cáncer, al año siguiente (2007) optó por un trasplante de células madre que buscaba cambiarle todo su tipo de sangre. Al mismo tiempo, valga decir, Brown se ofreció como voluntario en un protocolo experimental contra el VIH.
Como se sabe, el trasplante de células madre implicaba también el uso de medicamentos para eliminar las células naturales que produce la sangre y luego ser reemplazadas por el nuevo tejido, con posibilidad de originar todas las células hemáticas (de la sangre), pero a partir de un donante.
Hasta aquí, este procedimiento era igual a cualquier trasplante de médula ósea. Sin embargo, el protocolo experimental incluía, además de suspender los medicamentos antirretrovirales y someterse a quimioterapia, escoger entre los casi 300 donantes que se presentaron a uno que especialmente había heredado, tanto por vía materna como paterna, una mutación genética que en teoría prevenía la infección del VIH.
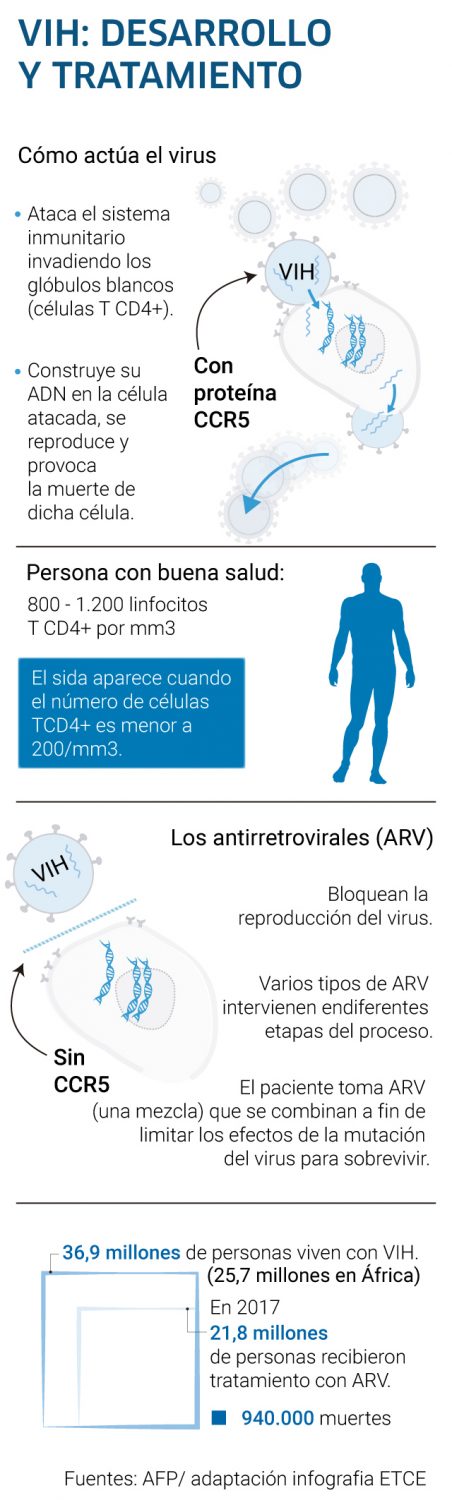
En otras palabras, el grupo investigador ya sabía de la existencia de ese gen que impedía que el virus entrara a las células de defensa de personas sanas y pensaba aprovecharlo. Dicho gen es el CCR5 Delta 32m, que en las células T CD4 (las que más se afectan) le cierra la puerta al VIH, al parecer porque carece de receptores específicos sobre los cuales se pueda adherir el virus.
Esta variante genética hace que los individuos que la poseen vean afectado el gen del receptor de la proteína CCR5 sobre las células sanguíneas de defensa. Hace varias décadas se planteó la hipótesis de que esta mutación proporcionaba resistencia a la peste bubónica en la Edad Media, sobre la base de que por la época en que apareció esta epidemia en Europa hubo personas que no se afectaron.
Aunque la hipótesis sobre la peste resultó falsa, la mutación exacta del CCR5 Delta 32m se identificó concretamente en el año 1996 en individuos que, a pesar de haber estado expuestos al virus del sida, parecían estar protegidos, incluso después de haber tenido contacto con él en repetidas ocasiones.
En estas personas se comprobó que carecían de receptores CCR5 en sus linfocitos CD4. Más tarde también se observó que aquellos con el gen, pero que no lo habían recibido conjuntamente por padre y madre (heterocigotos), tenían mejor pronóstico clínico frente al virus del sida que otros.
En experimentos posteriores se infectaron ratones portadores y no portadores del gen y se encontraron diferencias significativas frente al VIH, aunque se sigue pensando que la causa de la mutación que genera inmunidad fue la exposición a una enfermedad en la Edad Media, tal vez la viruela.
Todo esto para contar que en el caso de Timothy Brown, este procedimiento experimental resultó exitoso y aun hoy el llamado paciente Berlín es activista sobre prevención contra el VIH y vive sin tomar antirretrovirales.
El paciente Londres
Pero el asunto no paró ahí porque esta semana, la prestigiosa revista científica Nature sorprendió con un anuncio similar: una segunda persona en el mundo había logrado erradicar todo rastro del virus del VIH en su organismo gracias a otro trasplante de células madre.
Aunque en este caso se reservó la identidad, la investigación lo denominó como el paciente Londres y a continuación dio detalles, como que fue diagnosticado de VIH en el 2003 y seguía una terapia antirretroviral desde el 2012. Ese mismo año fue diagnosticado de un linfoma de Hodgkin avanzado (otra enfermedad cancerosa de la sangre no relacionada) por el que se sometió a un trasplante de células madre en el 2016.
A los 16 meses del trasplante, los médicos interrumpieron el tratamiento antirretroviral y al día de hoy, 18 meses después, el virus permanece indetectable en su sangre, pese a que, habitualmente, cuando las personas con infección por el VIH interrumpen el tratamiento, el virus reaparece en las cuatro primeras semanas.
No sobra decir que, de acuerdo con la información que ha trascendido, el protocolo aplicado en este segundo paciente fue menos intenso, más ordenado y, por ende, menos traumático que en el de su antecesor.
De acuerdo con Anne-Marie Wensing, viróloga del centro médico universitario de Utrecht, en los Países Bajos, y una de las coautoras del estudio, dicho paciente también recibió la donación de células con la mutación CCR5 en mayo del 2016 y al observar los resultados le dijo al New York Times que “esto inspirará a las personas para que piensen que curarse no es un sueño”, bajo la premisa de que las células inmunes trasplantadas parecen haber reemplazado completamente los linfocitos vulnerables del paciente de Londres.
El gen de la esperanza
Hay que reconocer que la base de estos avances promisorios está en un gen mutado (el CCR5 Delta 32m) que hasta ahora se ha encontrado en personas con ascendencia en el norte de Europa. Se sabe, por ejemplo, que un consorcio de científicos europeos tiene una base de datos con aproximadamente 22.000 donantes con esta mutación.
De igual manera, se conoció que el mismo grupo de investigación rastrea a 38 personas portadoras del virus del VIH que han recibido trasplantes de médula ósea, seis de las cuales no tienen el gen para hacer comparación.
De ese grupo, el 36 de la lista era el paciente de Londres, y el número 19, que al parecer va por el mismo camino, tiene resultados clínicos que serán dados a conocer la semana entrante y ya se conoce como el paciente de Düsseldorf.
En justas proporciones
No se puede desconocer la importancia de estos avances, pero los mismos investigadores son los primeros en enviar un mensaje de prudencia bajo la premisa de que replicar estos tratamientos tiene riesgos que son menores frente a los fármacos que hoy existen para controlar efectivamente la infección.
Lo que sí es cierto es que se abre la puerta para desarrollar terapias génicas que eliminen el CCR5 (los receptores) en las células de defensa. Estas células modificadas podrían limpiar la sangre del paciente.
Paradójicamente, la modificación de esta misma proteína fue la que trabajó el científico chino He Jiangkui, quien hace poco dijo haber editado genéticamente a dos gemelas. Y, por supuesto, se debe recordar que hay varias cepas del VIH, como la X4, que utilizan otras proteínas para ingresar a las células.

